امروزه در پزشکی از نور درمانی برای معالجه اختلال خلقی فصلی ، پسوریازیس و بقیه بیماریها استفاده می شود.در حالیکه لیزرهایی با نیروی هدف گیری بالا برای معالجه اختلالات و امراض پوستی، امراض چشمی و سرطان استفاده می شوند. پیشرفت های حاصل در روش های تصویربرداری و ابزارهای مربوطه به دانشمندان اجازه داده است تأثیر استفاده از نور را در سطح سلولی بررسی کنند. این فرصت سبب تغییر روش های تحقیقاتی در استفاده ی انواع ویژه ای از نور برای دستکاری مستقیم و پیچیده ی سلولها شده است.
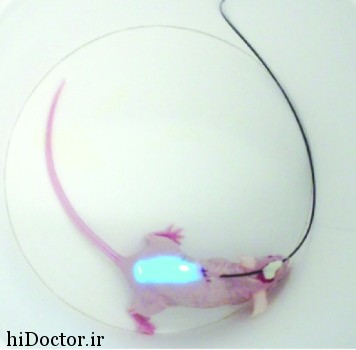
یک موش که آزادانه در حال حرکت است با یک هیدروژل کاشته شده در بدن همراه با یک کابل فیبر نوری. نور آبی که از طریق کابل دریافت می شود بوسیله ی هیدروژل بصورت یکسان توزیع می گردد.
اپتوژنتیک یک تکنیک نسبتاٌ جدید است که در آن از نور برای فعال سازی یا ممانعت از پروتئین های پاسخ دهنده به نور که اعمال خاص سلولی را کنترل می کنند، استفاده می شود.اکثر تحقیقات اپتوژنتیک تاکنون بروی هدف قرار دادن سلولهای مغزی صورت گرفته است این کار به دانشمندان کمک می کند تا به دستکاری نرون های افراد پرداخته و تأثیرات آنرا مشاهده نمایند. اما استفاده از این ابزار پیشگامانه برای مطالعه ی عملکرد داخلی مغز بدون نیاز به الکترود یا هرگونه تماس مستقیم با بافت مغز تبدیل به چالشی شده است که دلیل آن تاباندن نور به اعماق بدن است که استفاده ی گسترده تر از اپتوژنتیک را در بدن محدود کرده است.
در اکثر استفاده های بالینی که استفاده از نور در آنها پیشنهاد می شود باید نور به طور مساوی به تعدادی از سلولها تابانده شود تا تأثیر درمانی قابل تکرار باشد، اما بافت بدن انسان شفاف نبوده و نور را پراکنده و جذب می کند و بهر حال سبب کاهش نفوذ نور به داخل بدن شده و توانایی عبور نور در زیر پوست را کاهش می دهد. برای حل این مشکل ، پرفسور yun و محققین دانشکده ی پزشکی هاروارد و چندین انستیتوی تحقیقاتی در کره استفاده از هیدروژل شفاف با تکنیک اپتوژنتیک را آزمایش کردند.
هیدروژل در مفهوم عادی همانند ژلاتین خوراکی است اما برای ایمپلنتهای پزشکی توسط محققین استفاده می شود. در حال حاضر اکثر ایمپلنت های پزشکی از مواد سختی مانند پلاستیک و فلز ساخته می شوند اگر چه چنین ایمپلنت هایی با دقت فراوان برای انجام وظایفی در بدن طراحی شده اند اما بطور طبیعی استفاده از اجسام سخت در میان بافتهای نسبتاٌ نرم می تواند سبب ایجاد التهاب و سایر عوارض جانبی ناخواسته شود. درمقابل هیدروژل ها می توانند به آسانی با استفاده از مواد سازگار زیستی ساخته شده و به دلیل محتوای بالای آب آنها و طبیعت انعطاف پذیری که دارند بیشتر با ماهیچه ها، ارگانها و سایر بخش های داخلی بدن مطابقت داشته و قادر به هدایت نور بطور موثرتری هستند.
برخی از مایعات می توانند از میان هیدروژلها عبور کنند این قابلیت سبب می شود از این هیدروژل ها در انواع مختلفی از کاربردها که قبل از این با ساخت ایمپلنت هایی از مواد نفوذ ناپذیر انجام می شد، استفاده شود.
آزمایش با هیدروژل ها سبب شد دکترyun و همکارانش باریکه ای از هیدروژل انعطاف پذیر و شفافی را ابداع کنند که قادر به هدایت پرتولیزر و هدایت نور به جلو یا بازگشت نور در محدوده ای که قرار گرفته است، باشد.
محققین توانستند این هیدروژل را در سلولها جاگذاری نمایند ( مانند قطعات میوه درون دسر ژلاتینی) این هیدرروژلها قادر به منعکس کردن یا پراکنده کردن نور، ایجاد یک تابش یکنواخت از میان باریکه ی هیدروژل هستند.
هنگامیکه هیدروژل با یک فیبر نوری روشن می شود و درست زیر پوست موش کاشته می شود بوضوح قابل مشاهده و درخشان است.
در آزمایش پیگیری، محققان سلولهایی را پرورش دادند که در حضور کادمیوم که یک فلز سنگین سمی است و در تولید سنسورهای نقطه ای کوانتومی استفاده می شود نور سبز از خود ساتع می کردند. هنگامیکه نقاط کوانتومی با هسته ی کادمیوم به بدن موشهایی که دارای هیدروژل ایمپلنت هستند تزریق گردید سلولها در هیدروژل به رنگ سبز می درخشیدند. هنگامیکه نقاط مذکور با ماده ی سازگارتر زیستی یعنی زینک ( روی ) پوشش داده وتزریق گردید، هیدروژل دیگر تابش نکرد، این نشان می دهد پوشش زینک بطور موثر سلولها را در هیدروژل از کادمیوم محافظت می کند.
به منظور آزمایش تحویل دارو توسط هیدروژل، دانشمندان باریکه هایی از هیدروژلها ساختند که می توانستند آنها را در داخل سلولها وارد کنند این هیدروژل ها در حضور کلسیم می درخشیدند. این باریکه ها سپس به یک فیبر نوری آبی متصل شده و آنرا در موشی که با مواد شیمیایی بطور مصنوعی به دیابت مبتلا شده بود، کاشتند. هنگامیکه موش در معرض نور آبی قرار می گرفت پروتئینی بنام melanopsin سبب بروز آبشاری از فعالیت ها درون سلول می شد از جمله آزاد سازی کلسیم که به کنترل تأثیرات دیابت کمک می کند.
در موشهایی که در معرض نور آبی قرار گرفته بودند ، سلولهایی که در هیدروژل ایمپلنت قرار داشتند بیش از سلولهایی که در هیدروژل موشهایی که در معرض نور آبی نبودند، می درخشیدند. این موضوع نشان می دهد در گروه اول مقدار کلسیم داخل سلولی بیشتر بوده و فعالیت ضد دیابتی بیشتری دارد.
برای اثبات اعتبار این یافته ها، موشها تحت تست تحمل گلوکز قرار گرفتند تا مدت زمانیکه طول می کشد تا مقدار قند خون آنها به حالت طبیعی برگردد آزمایش شود- از آنجائیکه دیابت توانایی بدن را در فرآوری قند خون مختل می کند مقدار قند خون افراد دیابتی نسبت به افراد طبیعی مدت زمان بیشتری بالا می ماند.
در موشهای دیابتی در معرض نور مقدار قند خون در طی یک ساعت ونیم به حالت طبیعی برگشت درحالیکه در موشهای دیابتی که در معرض نور نبودند، مقدار قند خون بعد از گذشت 2 ساعت همچنان بالا بود. این نشاندهنده ی تأثیر نور تحویل داده شده از طریق هیدروژل و تولید تأثیرات بیولوژیک قابل اندازه گیری آن است که ممکن است روزی به ابزاری مفید برای تحویل درمان بروش اپتوژنتیک تبدیل گردد.
با ارئه ی نور در داخل بدن به شیوه ای کنترل شده و قابل پیش بینی و مهندسی ژنتیک بروی سلولهای میزبان بنحوی که قادر به پاسخگویی به نور بوده یا توانایی عبور نور در پاسخ به یک سیگنال شیمیایی ویژه ای را داشته باشند می توان به برخی از چالش های موجود بر سر راه استفاده از روش های اپتوژنتیک در مراقبت های کلینیکی فائق آمد.
پرفسور conroyمی گوید: برای اعتبار بیشتر و پالایش و بهبود این تکنولوژی قبل از استفاده از آن در مسائل مربوط به سلامت انسان، نیاز به تحقیقات بیشتری داریم اما نتایج این تحقیق برای پیشبرد درمانهای پزشکی مبتنی بر نور بسیار امیدوار کننده است.
منبع-http://diabetestma.org