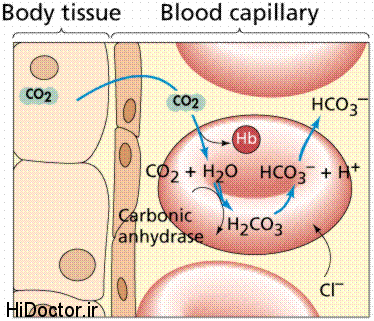
علاوه بر اندازه های مربوط به Pao2 و o2 Sat ، ببقیه اندازه ها که برای شرح اختلالات اسید باز مورداحتیاج است ، حاوی اندازه های PH ، PaCo2 ، HCo3 ، Base Excess (BE) ، Total Co2 Conent ، BD و Anion Gap است .
علاوه بر اندازه های مربوط به Pao2 و o2 Sat ، ببقیه اندازه ها که برای شرح اختلالات اسید باز مورداحتیاج است ، حاوی اندازه های PH ، PaCo2 ، HCo3 ، Base Excess (BE) ، Total Co2 Conent ، BD و Anion Gap است .
PH :
PaCo2 :
HCo3 :
Base Excess – BE :
همانگونه که پیشتر گفته شد ، PH نمایانگر وضعیت یک محلول از نظر اسید – باز است . PH طبیعی خون بین ۷٫۳۵ تا ۷٫۴۵ است و بطور متوسط میزان آن را ۷٫۴۰ در نظر می گیرند . به PH بالاتر از ۷٫۴۵ آلکالمی و به PH زیر ۷٫۳۵ اسیدمی گفته می شود . تغییرات PH عکس تغییرات غلظت یون هیدروژن (H) است .
ph2
نمایانگر میزان دی اکسید کربن موجود در خون شریانی است . این گاز توسط متابولیسم سلولی ساخته شده ، از طریق ریه ها دفع می گردد . میزان طبیعی آن بین ۳۵ – ۴۵ میلیمتر جیوه و بطور متوسط ۴۰ mmHg است . هرگونه تغییر در مقدار PaCo2 منجر به بروز خواهد شد . افزایش این میزان از ۴۵ میلیمتر جیوه را اسیدوز تنفسی و کاهش آن از ۳۵ میلیمتر جیوه را آلکالوز تنفسی گویند . تغییرات Paco2 نسبت عکس با تغییرات غلظت یون هیدروژن دارد .

ABG2
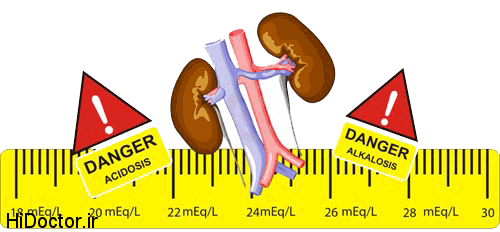
غلظت یون بیکربنات یک پارامتر متابولیک محسوب می شود و تغییرات آن بیانگر وجود اسیدوز یا آلکالوز متابولیک است . میزان طبیعی یون بیکربنات بین ۲۲ تا ۲۶ mEq/L و یا بطور متوسط ۲۴ mEq/L است . افزایش آن از ۲۶ mEq/L بیانگر آلکالوز متابولیک و کاهش آن از ۲۲ mEq/L بیانگر اسیدوز متابولیک است . تغییرات بیکربنات نسبت مستقیم با تغییرات حاد دارد .
ABG3
در شرایطی که PaCo2 در حرارت ۳۷ درجه سانتی گراد ، معادل ۴۰ mmHg بوده ، کمبود اکسیژن نیز وجود نداشته باشد ، BE به مقدار اسید یا بازی اطلاق می گردد که برای حفظ PH در حد طبیعی و نیز حفظ بیکربنات به میزان ۲۴ mEq/L مورد نیاز است . به عبارت دیگر مقدار BE وابسته به تجمع اسید یا باز غیر فرار در خون است . مقدار طبیعی BE بین ۲+ و ۲- متغیر بوده و بر حسب mEq/L ( میلی اکی والان در لیتر ) بیان می شود .
افزایش BE از ۲+ نمایانگر احتباس باز غیر فرار و یا به عبارت دیگر آلکالوز متابولیک ، و کاهش BE از ۲- نمایانگر احتباس اسید غیر فرار و یا به عبارت دیگر اسیدوز متابولیک است .
در مواردی که BE ، ارقام منفی نشان می دهد ( یعنی وجود اسیدوز متابولیک ) بهتر است از واژه Base Deficit – BD استفاده شود .
Buffer Base – BB :
Total Co2 – Tco2 :
Anion Gap – AG :
یک معیار تشخیصی برای تغییرات متابولیک اسید – باز است و هنگامی بکار برده می شود که تعادل اسید – باز با تعادل الکترولیتها مورد مقایسه قرار گیرد . در واقع BB حاصل جمع آنیونهای پلاسما یعنی بیکربنات ، پروتئین ، هموگلوبین و فسفاتها بوده ، مقدار آن معادل ۴۲ میلی مول در لیتر است . رابطه ساده ای بین BE و BB پلاسما وجود دارد که عبارتست از : BB = BE+42 و از آنجایی که BE پلاسما در حالت تعادل تقریبا برابر صفر است ، BB = 42 خواهد بود . در صورت بروز آلکالوز متابولیک مقدار آن افزایش یافته ، در صورت ایجاد اسیدوز متابولیک ، از میزان آن کاسته می شود ، تغییرات Co2 خون شریانی تاثیر روی مقدار BB ندارد .
میزان کل Co2 عبارتست از مجموع غلظت یون بیکربنات ، اسید کربنیک و دی اکسید کربن موجود در خون . چون حدود ۹۸% از میزان کل Co2 را یون بیکربنات تشکیل می دهد ، این میزان تقریبا برابر با مقدار یون بیکربنات ، یعنی حدود ۲۵٫۲ mEq/L است .
طبق قانون تعادل الکتروشیمیایی ، همواره تعداد کل آنیون ها ، با تعداد کل کاتیون ها برابر و در حالت تعادل است . کاتیون های قابل اندازه گیری شامل یونهای سدیم و پتاسیم بوده ، و آنیون های قابل اندازه گیری شامل یونهای کلر و بیکربنات هستند . AG عبارت از تفاضل آنیون ها و کاتیون های سرم بوده ، بعنوان کمکی برای کشف علت اسیدوز متابولیک بکار گرفته می شود . برای محاسبه آن باید غلظت یون سدیم را از مجموع یون های کلر و بیکربنات کم نمود ( غلظت یون پتاسیم را در نظر نمی گیرند )
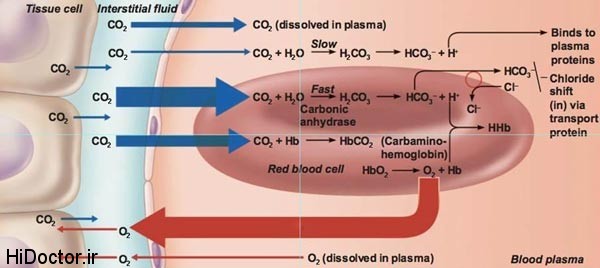
مقدار طبیعی AG بین ۸ تا ۱۶ و به طور متوسط ۱۲ mEq/L است . کاهش AG در هیپوآلبومینمیا ، افزایش آب ، یا میلوم مولتیپل دیده می شود . افزایش AG که بسیار شایعتر است در اسیدوز متابولیک ملاحظه می گردد . همانطور که قبلا توضیح داده شد ، اسیدوز متابولیک دارای دو علت عمده است :
کاهش یون بیکربنات
افزایش اسید
در بیماری که دچار اسیدوز متابولیک ناشی از کاهش یون بیکربنات شده است ، AG در حد طبیعی است . در بیماری که دچار احتباس اسید های حاوی کلر می شود ( نظیر HCL و NH4Cl ) نیز AG در حد طبیعی است . اما در بیماری که دچار افزایش اسید های ارگانیک نظیر اسید لاکتیک و کتو اسید می شود ، شاهد افزایش AG خواهیم بود .
تغییرات AG در انواع اسیدوز متابولیک بصورت زیر خلاصه شده است :
افزایش AG
خوردن اسید ( نظیر مصرف آسپرین بیش از حد مجاز و خوردن متانول )
افزایش اسید های متالبولیک ( نظیر اسیدوز متابولیک )
متابولیسم غیر طبیعی یا ناقص ( نظیر کتواسیدوز )
اختلال در دفع اسید ( نظیر نارسایی شدید کلیه )
AG طبیعی
کاهش اولیه بیکربنات ( نظیر اسهال )
مصرف اسید های حاوی کلراید ( نظیر HCl و NH4Cl )
اختلال در دفع اسید ( نظیر بدکاری خفیف کلیه )
ABG3
gasexch_1 gasexch_2
روش تفسیر برگه آزمایش گاز های خون شریانی :
مراحل تفسیر ABG به قرار زیر است :
مرحله اول :
مشاهده مقدار PaO2 و O2 Sat به میزان PaO2 نگاه کرده و به این سوال در ذهن خود پاسخ دهید ، آیا PaO2 نمایانگر وجود هایپوکسمی است ؟ همانطور که پیشتر نیز گفته شد ، PaO2 به اکسیژن محلول در خون بر می گردد و در حالت طبیعی مقدار آن بین ۱۰۰ – ۸۰ mmHg است . PaO2 با تغییرات درجه حرارت بدن تغییر می کند . هرچه میزان درجه حرارت بدن افزایش یابد ، PaO2 کاهش می یابد . PaO2 بین ۶۰ تا ۷۹ mmHg را هایپوکسی خفیف ، بین ۵۹ – ۴۰ mmHg را هایپوکسی متوسط ، و کمتر از ۴۰ mmHg را هایپوکسی شدید می نامند . PaO2 پایین تر از ۴۰ mmHg به منزله یک موقعیت بسیار مخاطره آمیز برای بیمار در نظر گرفته می شود . البته مقادیر فوق همگی تقریبی بوده ، با وضعیت جسمی ، سنی و بیماری های زمینه ای فرد تغییر می کند . محاسبه ی تغریبی حداقل PaO2 طبیعی در افراد بالای ۴۰ سال :
2-PaO2
بطور تقریبی در افراد بالای ۶۰ سال ، می توان به ازای هر یک سال افزایش سن از ۶۰ سال ، ۱ میلیمتر جیوه از پایین ترین میزان طبیعی mmHg 80 PaO2 کم نمود تا حدود PaO2 طبیعی وی محاسبه شود . برای مثال اگر فردی ۷۵ سال سن داشته باشد ، حدود طبیعی PaO2 وی برابر ۶۵ mmHg خواهد بود . O2 Sat یا درصد اشباع هموگلوبین از اکسیژن نیز به مقدار PaO2 و عوامل موثر بر منحنی شکست اکسی – هموگلوبین وابسته است . در صورتی که O2 Sat زیر ۸۰% باشد ، احتمال اینکه نمونه خون تهیه شده وریدی باشد ، بسیار زیاد است ( مگر در افرادی که مبتلا به COPD باشند )
hemoglobin_dissociation_curve
مرحله دوم :
مرحله سوم :
مرحله چهارم :
مرحله پنجم :
مرحله ششم :
به سطح PH نگاه کنید و به این سوال در ذهن خود پاسخ دهید : آیا PH اسیدی یا قلیایی بوده و یا نرمال است ؟
PH نمایانگر غلظت یون هیدروژن در پلاسما است . PH کمتر از ۷٫۴۰ اسیدی تلقی می شود و در صورتی که PH کمتر از ۷٫۳۵ شود به آن اسیدمی یا اسیدوز اطلاق می گردد . PH بالاتر از ۷٫۴۰ نیز قلیایی تلقی می شود و در صورتی که بیشتر از ۷٫۴۵ شود به آن آلکالمی یا آلکالوز گویند .
به مقدار PaCO2 نگاه کنید و به این سوال در ذهن خود پاسخ دهید : آیا PaCO2 نشانگر اسیدوز تنفسی یا آلکالوز تنفسی بوده و یا طبیعی است ؟
مقدار طبیعی PaCO2 بین ۴۵ – ۳۵ mmHg است و تغییرات آن نسبت عکس با PH دارد . PaCO2 کمتر از ۳۵ mmHg را آلکالوز تنفسی و بیش از ۴۵ mmHg را اسیدوز تنفسی می نامند .
به میزان HCO3 توجه کرده در ذهنتان به این سوال پاسخ دهید : آیا HCO3 نمایانگر اسیدوز یا آلکالوز متابولیکی بوده و یا طبیعی است ؟
تغییرات HCO3 نسبت مستقیم با تغییرات PH دارد . مقدار طبیعی آن بین ۲۶ – ۲۲ mEq/L است . مقادیر بیش از ۲۶ mEq/L نمایانگر آلکلوز متابولیک و مقادیر کمتر از ۲۲ mEq/L نشان دهنده اسیدوز متابولیک است .
به مقدار BE توجه کنید و به این سوال در ذهن خود پاسخ دهید : آیا مقدار آن در حدود طبیعی است یا خیر ؟
این معیار ، در تفسیر علت اسیدوز – آلکالوز با منشا متابولیک ، معتبر تر و دقیق تر از یون بیکربنات است . در صورتی که بیش از ۲+ باشد نمایانگر آلکالوز متابولیک است و اگر کمتر از ۲- باشد نمایانگر اسیدوز متابولیک است .
مجددا به PH نگاه کنید و به این سوال در ذهن خود پاسخ دهید : آیا PH نمایانگر حالت جبران شده است یا بدون جبران ؟
همانطور که پیشتر نیز گفته شد در بدن مکانیزم های جبرانی ( بافری – تنفسی – متابولیکی ) در زمان اختلالات اسید و باز فعال شده سعی می کنند PH را به حد نرمال باز گردانند . در زمان تفسیر ABG ممکن است با یکی از ۳ حالت زیر روبرو شوید :
بدون جبران
جبران ناقص
جبران کامل
الف ) بدون جبران
در این حالت PH غیر طبیعی بوده PaCO2 یا HCO3 نیز غیر طبیعی هستند . در چنین وضعیتی با توجه به مقدار PH ، نوع اختلال ( اسیدوز یا آلکالوز ) مشخص می گردد و هر کدام از دو پارامتر دیگر یعنی PaCO2 یا HCO3 نمایانگر نوع اختلال ( تنفسی یا متابولیکی ) خواهند بود .
مثال ۱ : در برگه ABG مقادیر زیر مشاهده می شود :
PaO2 = 60 mmHg
PH = 7.25
PaCo2 = 50 mmHg
HCO3- = 22 mEq/L
در این این مثال با توجه به مقدار PH ، تشخیص اسیدوز داده می شود ، از آنجایی که مقدار بیکربنات طبیعی بوده و تنها PaCO2 افزایش نشان می دهد ( اسیدوز تنفسی ) تشخیص عبارت است از : آسیدوز تنفسی جبران نشده
مثال ۲ : در برگه ABG مقادیر زیر مشاهده می شود :
paO2 = 90 mmHg
PH = 7.25
PaCO2 = 40 mmHg
HCO3- = 17 mEq/L
در این مثال با توجه به مقدار PH ، تشخیص اسیدوز داده می شود و از آنجایی که PaCO2 نرمال بوده ، مقدار HCO3 کمتر از حد طبیعی است ، تشخیص عبارتست از : اسیدوز متابولیک جبران نشده .
ب ) جبران ناقص
در این حالت PH ، HCO3 و PaCo2 هر سه غیر طبیعی هستند . این حالت نمایانگر این است که مکانیزمهای جبرانی فعال شده ولی هنوز موفق به اصلاح کامل PH نشده اند . برای تشخیص علت اولیه ( اختلال اولیه ) و مکانیز جبرانی ، ابتدا با نگاه کردن به مقادیر HCO3 ، PaCO2 نوع اختلال را مشخص کرده ، سپس به مقدار PH نگاه می کنیم . در اینجا قانون اول مطرح می شود :
قانون I : اگر تغییرات PaCO2 و HCo3 هم جهت باشند ، بدن در حالت جبران عدم تعادل است .
مثال :
PH = 7.30 ↓
PaCo2 = 25 mmHg ↓
HCO3 – = 12 mEq/L ↓
تشخیص : اسیدوز متابولیک با جبران ناقص تنفسی
ج ) جبران کامل
در این حالت PH طبیعی ، ولی PaCO2 و HCO3 هر دو غیر طبیعی هستند . این حالت نمایانگر آن است که فعالیت مکانیزم های جبرانی موجب برگرداندن PH به سطح طبیعی شده است ، لیکن متعاقب جبران ، مقادیر نرمال PaCO2 و HCO3 – هر دو طبیعی هستند .
قانون II : در وضعیت جبران کامل ، برای تشخیص علت اولیه ( اختلال اولیه و مکانیزم جبرانی ) ابتدا یا نگاه کردن به مقادیر HCO3 – ، BE و PaCO2 نوع اختلال را مشخص کرده ، سپس به مقدار PH نگاه می کنیم :
در صورتیکه میزان PH بین ۷٫۳۵ – ۷٫۴۰ بوده ، علت اولیه اسیدوز است .
در صورتیکه میزان PH بین ۷٫۴۵ – ۷٫۴۰ بوده ، علت اولیه آلکالوز است .
مثال :
PH = 7.42
PaCO2 = 50 mmHg ↑
HCO3 – = 32 mEq/L ↑
تشخیص : آلکالوز متابولیک ، اسیدوز تنفسی ، جبران کامل .
بیماری اولیه : آلکالوز متابولیک ( با جبران کامل )
اختلالات مرکب اسید – باز ( Mixed Disorders )
در پاره ای مواقع ممکن است هر دو نوع اختلال تنفسی و متابولیکی در یک بیمار وجود داشته باشد . بسته به مقتضیات بالینی ، یک اختلال مرکب یا مخلوط می تواند بصورت دو نوع اسیدوز ، دو نوع آلکالوز یا یک نوع اسیدوز همراه یک نوع آلکالوز باشد .
موارد زیر نمونه هایی از این اختالات مرکب است :
اسیدوز تنفسی + آلکالوز متابولیک ( مثل COPD + استفراغ )
اسیدوز تنفسی + اسیدوز متابولیک ( مثل ایست قلبی – تنفسی + اسهال )
آلکالوز تنفسی + آلکالوز متابولیک ( مثل هایپرونتیلاسیون ناشی از درد یا عفونت + ترانسفوزیون مقادیر بالای خون )
اسیدوز متابولیک + آلکالوز متابولیک ( مثل نارسایی کلیه + اسهال ) مقادیر آزمایشگاهی بستگی به مدت و شدت هر کدام از اختلالات دارد .
دو نوع اسیدوز متابولیک توام ( مثل کتواسیدوز دیابتی + لاکتیک اسیدوز )
در کلیه وضعیت های بالا ، PH خون می تواند نشانگر وضعیت حاد ، تحت حاد و یا مزمن باشد . وضعیت حاد به حالتی بر می گردد که هنوز مکانیزم های جبرانی فعالیت چشمگیری از خود نشان نداده اند . در وضعیت تحت حاد ، مکانیسم های جبرانی فعال شده اند ، اما جبران بصورت نسبی صورت گرفته است و هنوز PH به میزان طبیعی نرسیده است و بالاخره در وضعیت مزمن ، جبران بصورت کامل صورت گرفته و PH خون به طبیعی رسیده است ، هر چند هنوز حالتهای اسیدوز و یا آلکالوز تنفسی و متابولیک وجود دارند .
مثال :
PH = 7.20 ↓
PaCO2 = 55 mmHg ↑
HCO3 – = 20 mEq/L ↓
در این مثال PH نمایانگر حضور یک اسیدوز شدید است . PH و PaCo2 در جهت مخالف یکدیگر تغییر کرده اند ، که دلیل بر وجود یک بیماری تنفسی است . اما تغییرات PH و HCO3 – در جهت یکدیگر ( هم جهت ) است . بنابراین یک بیماری متابولیکی نیز وجود دارد . در کل مقادیر مذکور نشانگر یک اسیدوز مرکب ( Mixed ) تنفسی و متابولیک است . مثال بالینی برای این حالت ، ایست قلبی – ریوی است که در آن بعلت تهویه ناکافی و تجمع Co2 ، اسیدوز تنفسی ایجاد می شود و بدلیل اکسیژناسیون ناکافی بافتی و تجمع اسید لاکتیک ، اسیدوز متابولیک حاصل می گردد .
بنابراین :
اگر PaCO2 و HCO3 در جهت مخالف یکدیگر تغییر نمایند ، بیمار دچار یک عدم تعادل مرکب است .”
تغییرات در PH و PaCO2 و بی کربنات ( HCO3 )
زمانیکه مقدار PaCO2 در خون افزایش یابد ، PH خون اسیدی تر می شود . با شناخت PH و PaCO2 می توان مضعیت بیمار را ارزیابی کرده و علل عدم ثبات در تعدال اسید و باز را مشخص نمود . با توجه به معادله هاندرسن هاسلباخ ارتباط بین PH و PaCO2 و بی کربنات به صورت زیر می باشد .
3-handersen 4-handersen
غلظت یون هیدروژن بر حسب نانومول در لیتر ( Nm/L ) بوده و عدد ۲۴ حاصل از تجزیه اسید کربنیک می باشد . در جدول زیر ارتباط PH و غلظت یون H نشان داده شده است . زمانیکه غلظت یون H محاسبه شد ، با نگاه به جدول می توانید PH را تعیین کرد .
مثال :
PaCO2 = 50
HCO3 – = 24
H = ?
7-mesal1
با توجه به جدول ، در غلظت یون H به میزان PH ، ۵۰ nm/l نزدیک به ۷٫۳۰ خواهد بود .
مقدار بی کربنات سرم را نیز می توان با استفاده از معادله زیر می توان با استفاده از معادله زیر بدست آورد :
5-mesal1
مثال :
PH = 7.40
PaCO2 = 50
HCO3 – = ?
6-mesal2
مقادیر بدست آمده ، تخمینی از مقدار واقعی بوده و در موقعیت های بالینی برای تعیین سریع مقادیر بی کربنات ، PH و PaCo2 ، با دانستن مقادیر دو فاکتور دیگر قابل استفاده می باشد .
مقادیر بدست آمده ، تخمینی از مقدار واقعی بوده و در موقعیت های بالینی برای تعیین سریع مقادیر بی کربنات ، PH و PaCo2 ، با دانستن مقادیر دو فاکتور دیگر قابل استفاده می باشد .
افتراق هایپر کاپنی حاد از مزمن
جهت افتراق هیپر کاپنی حاد از مزمن ابتدا بایستی دامنه تغییرات یون هیدروژن ( H ) نسبت به دامنه تغییرات PaCo2 تعیین شود . این نسبت در حالات مختلف هیپر کاپنی به قرار زیر است : در هیپر کاپنی حاد نسبت در حدود ۰٫۷ و در هیپر کاپنی مزمن در حدود ۰٫۳ یا کمتر و در هیپر کاپنی حاد در زمینه مزمن ، بین ۰٫۳ تا ۰٫۷ می باشد .
مثال ۱ : اگر
HCO3 = 28 mEq/lit ، PaCo2 = 80 mmHg و PH = 7.19 باشد نوع اختلال را مشخص نمایید :
10-mesal1
با توجه به غلظت [ H ] که در PH طبیعی ( ۷٫۴ ) مساوی ۴۰ Nm/L است در این حالت دامنه تغییرات [ H ] معادل ۲۸ خواهد شد .
H = 68 – ۴۰ = ۲۸ ∆
همچنین دامنه تغییرات CO2 نسبت به CO2 طبیعی ۴۰ می باشد .
CO2 = 80 – ۴۰ = ۴۰ mmHg∆
نسبت دامنه تغییرات H به CO2 به قرار زیر است :
11-mesal1
با توجه به عدد حاصله ( ۰٫۷ ) ، این حالت نمایانگر هیپرکاپنی حاد می باشد .
مثال ۲ : اگر HCO3 = 38 ، PaCo2 = 92 و PH = 7.25 باشد . نوع اختلال را مشخص نمایید .
12-mesal2
با توجه به عدد حاصله ( ۰٫۳۵ ) که بین ۰٫۳ تا ۰٫۷ است ، این حالت نمایانگر هیپر کاپنی حاد در زمینه مزمن است .
روش توصیف شده در ارزیابی هیپرکاپنی و ارتباط بین PH ، PaCo2 و بی کربنات به افتراق انواع هیپر کاپنی ارزشمند است . زیرا هر نوع اختلال نیازمند درمان خاص بوده و افتراق بالینی آن بسیار مهم می باشد .
ایجاد تغییرات در PH ناشی از تغییرات PaCo2
زمانیکه مقدار CO2 خون افزایش می یابد به ازای هر ۲۰ mmHg افزایش در مقدار CO2 ، مقدار PH به میزان ۰٫۱ کاهش می یابد .
مثال :
PaCO2 = 40 → PH = 7.40
PaCO2 = 60 → PH = 7.30
PaCo2 = 80 → PH = 7.20
زمانیکه مقدار CO2 کاهش می یابد ، به ازای هر ۱۰ mmHg کاهش در مقدار Co2 ، مقدار PH به میزان ۰٫۱ افزایش می یابد . اگر PaCO2 = 80 باشد مقدار CO2 به میزان ۴۰ mmHg بالاتر از حد نرمال است در این حالت اگر PH حدود ۰٫۲ کاهش نشان دهد و به ۷٫۲۰ رسیده باشد این تغییر در PH ناشی از هیپوونتلاسیون بطور خالص بوده ، در غیر اینصورت مشکل متابولیکی نیز وجود خواهد شد .
مثال :
PaCO2 = 30 → PH = 7.50
PaCO2 = 20 → PH = 7.60
اگر PaCo2 = 20 باشد ، مقدار CO2 به میزان ۲۰ mmHg پایین تر ازحد نرمال است . در این حالت اگر PH حدود ۰٫۲ افزایش یافته و به ۷٫۶۰ رسیده باشد ، این تغییر در PH ناشی از هیپرونتیلاسیون خواهد بود . در غیر اینصورت مشکل متابولیکی نیز وجود دارد . با استفاده از این روش می توان تعیین نمود که آیا تغییرات PH انعکاسی از تغییرات CO2 است (مشکلات خالص تنفسی) یا بعلت تغییرات متابولیکی همراه شده با مشلات تنفسی می باشد (Mixed)
در حالت دوم اگر PH به جای ۷٫۶۰ معادل ۷٫۵۰ بود می توان نتیجه گرفت که تغییر در PH تنها علل تهویه ای نداشته و می تواند نمایانگر یک اختلال مرکب ( MIX ) شامل اسیدوز متابولیک همراه با آلکالوز تنفسی می باشد .
ایجاد تغییرات بی کربنات پلاسما ناشی از تغییرات PaCO2
بالا رفتن CO2 در خون موجب تولید اسید کربنیک و افزایش غلظت یون H و بی کربنات ( HCO3 ) می شود . ( طبق رابطه زیر ) :
HCO3 CO2 + H2O ↔ H2CO3 ↔ H + HCO3
در ضمن هیپوونتیلاسیون ، به ازای هر ۱۰ mmHg افزایش در PaCo2 مقدار بی کربنات به میزان ۱mEq/Lit افزایش می یابد و در ضمن هیپرونتیلاسیون کاهش در PaCO2 به میزان ۱۰mmHg موجب کاهش در بیکربنات سرم به میزان ۱٫۵ mEq/Lit خواهد شد .
مثال : اگر PaCo2 = 40 و HCO3 = 24 باشد و PaCo2 به ۵۰ mmHg افزایش یابد ، بیکربنات نیز به ۲۵ mEq/lit افزایش خواهد یافت و در صورتیکه PaCo2 به ۲۰ mmHg کاهش یابد HCO3 به ۲۱ mEq/lit کاهش می یابد .
اگر هیپوونتیلاسیون یا هیپرونتیلاسیون برای ۲ تا ۳ روز ادامه یابد و کلیه ها دارای عملکرد طبیعی باشند ، اختلال PH ناشی از مشکلات تنفسی با جبران کلیوی از طریق احتباس یا دفع HCO3 جبران خواهد شد .
همانطور که در مثال بالا ذکر شد ، در صورتیکه PaCO2 = 50 شود ، بیکربنات مساوی ۲۵ mEq/lit خواهد شد . اگر هیپوونتیلاسیون موجب یگ اسیدوز تنفسی شده باشد .
کلیه ها با حفظ حدود ۲ mEq/lit بی کربنات دیگر به ازای هر ۱۰ mmHg افزایش CO2 ، آن را جبران می نماید در این حالت بی کربنات سرم ، به ۲۷ mEq/lit افزایش خواهد یافت . از طرف دیگر در ضمن هیپرونتیلاسیون ، کلیه ها آن را از طریق دفع بی کربنات به میزان ۳ mEq/Lit به ازای هر ۱۰ mmHg کاهش در PaCO2 جبران می نمایند .
طبق مثال بالا ، PaCO2 = 20 بیکربنات ۲۱ mEq/lit می شود که با جبران کلیوی بایستی بی کربنات به ۱۵ mEq/lit برسد .
تغییرات بی کربنات و PH به دلیل تغییرات متابولیکی
تغییر در P H به میزان ۰٫۱۵ موجب تغییر در باز به میزان ۱۰ mEq/lit خواهد شد . در صورتیکه علت آن به طور خالص متابولیک باشد .
مثال : اگر PH از ۷٫۴۰ به ۷٫۵۵ افزایش یابد ( به میزان ۰٫۱۵ ) در این حالت بی کربنات بایستی به میزان ۱۰ mEq/lit افزایش یابد ( اگر باز ابتدا نرمال بوده باشد ) و بی کربنات به ۳۴ mEq/lit برسد تا جبران شود . اگر PH از ۷٫۴۰ به ۷٫۲۵ افت کرده باشد ، انتظار داریم به ازای ۰٫۱۵ کاهش در PH ، بی کربنات به میزان ۱۰ mEq/lit کاهش یافته و به ۱۴ mEq/lit رسیده باشد . در غیر ایصورت مشکل تنفسی نیز توام با مشکل متابولیکی وجود دارد (mixed) .
سخن نویسنده
دوستان و همراهان عزیز ایستگاه پرستاری امیدوارم مطلب حاضر مورد رضایت و استفاده شما عزیزان قرار گرفته باشد . این مطلب در نسخه قبلی ایستگاه پرستاری بیش از ۴۱۰۰ بار بازدید شده بود که نشان دهنده اهمیت و توجه موضوع در نظر شما عزیزان دارد . سعی اینجانب بر این بود که مطلب ساده ، روان و قابل فهم باشد . لطفا ما را از نظرات و راهنمایی های خود محروم نفرمایید .
منبع -http://nurse-station.ir/
راهنمای بالینی پاشا : تفسیر ABG ( دکتر حجت اله اکبر زاده پاشا )