قرنیه یک لایه روشن در قسمت جلوی چشم است که به تجمع نور کمک می کند تا بتوانید به وضوح مشاهده کنید. اگر آسیب ببیند، ممکن است نیاز به تعویض آن داشته باشید. جراح تمام یا بخشی از قرنیه شما را برداشته و آن را با یک لایه سالم از بافت قرنیه دیگر جایگزین می کند. قرنیه جدید از طرف افرادی دریافت می شود که هنگام فوت، این بافت را اهدا کردند. پیوند قرنیه ، که به آن کراتوپلاستی نیز گفته می شود، می تواند باعث به وجود آمدن بینایی و کاهش درد شود. برای آشنایی بیشتر درباره جراحی پیوند قرنیه ادامه این مقاله از چشم و چشم پزشکی دکتر سلام را مطالعه نمایید.
چه کسانی به پیوند قرنیه احتیاج دارند؟
پرتوهای نوری که از طریق قرنیه آسیب دیده عبور می کنند می توانند تحریف شده و دید شما را تغییر دهند. پیوند قرنیه چندین مشکل چشم را اصلاح می کند، از جمله:
- زخم قرنیه به دلیل آسیب یا عفونت
- زخم های قرنیه یا “زخم” ناشی از عفونت
- یک وضعیت پزشکی که باعث بیرون زدگی قرنیه شما می شود (کراتوکونوس)
- نازک شدن، گرفتگی یا تورم قرنیه
- بیماری های ارثی چشم مانند دیستروفی فوچ
- مشکلات ناشی از عمل زودرس چشم
پزشک پیوند قرنیه به شما اطلاع می دهد کدام روش خاص برای وضعیت شما بهتر است.
پیوند قرنیه با ضخامت کامل
اگر پزشک کراتوپلاستی نافذ (PK) انجام دهد، تمام لایه های قرنیه شما جایگزین می شوند. جراح پیوند قرنیه جدید را با استفاده از بخیه،روی چشم شما قرار می دهد. در صورت آسیب دیدگی قرنیه یا ضعف زیاد و زخم ممکن است به این روش احتیاج داشته باشید.
پیوند قرنیه با ضخامت جزئی
در حین عمل جراحی پیوند قرنیه عمیق (DALK)، جراح برای بلند کردن و جدا کردن لایه های نازک بیرونی و ضخیم میانی قرنیه، هوا تزریق می کند، سپس آنهایی را که جدا کرده، جایگزین می کند. ممکن است افراد مبتلا به کراتوکونوس یا زخم قرنیه که لایه های داخلی را تحت تأثیر قرار نداده است، این جراحی را انجام دهند. زمان بهبودی با این روش کوتاه تر از پیوند با ضخامت کامل است. از آنجا که قرنیه چشم شما کامل باز نشده است، بعید به نظر می رسد که لنز و عنبیه آسیب دیده باشد، و احتمال ابتلا به عفونت در چشم شما کمتر است.
جراحی پیوند قرنیه اندوتلیال
در حدود نیمی از افرادی که هر سال نیاز به پیوند قرنیه دارند، با لایه داخلی قرنیه، اندوتلیوم مشکلی ندارند. پزشکان معمولاً برای کمک به دیستروفی فوکس و سایر شرایط پزشکی این نوع جراحی را انجام می دهند.جراحی پیوند قرنیه اندوتلیال سلب شده Descemet (DSEK یا DSAEK) رایج ترین نوع جراحی پیوند قرنیه اندوتلیال است. جراح اندوتلیوم – که فقط یک سلول ضخیم دارد – و غشای Descemet را که دقیقاً بالای آن است از آن جدا می کند. سپس او آنها را با یک اندوتلیوم و غشای Descemet اهدا شده که هنوز به استروما متصل است (لایه میانی ضخیم قرنیه) تعویض می کند تا به وی به بافت جدید بدون آسیب رساندن به آن کمک کند.
تغییر دیگر، جراحی پیوند قرنیه اندوتلیال غشایی (DMEK)، پیوند فقط غشاء اندوتلیوم و Descemet – بدون استرومای پشتیبانی کننده است. بافت اهدا کننده بسیار نازک و شکننده است، بنابراین کار با آن سخت تر است، اما بهبودی این روش معمولاً سریعتر است. گزینه سوم برای افراد منتخب با دیستروفی فوچ، برداشتن ساده قسمت مرکزی غشای داخلی و بدون پیوند است. این جراحی ها فقط برای افراد آسیب دیده در قرنیه گزینه های خوبی هستند زیرا بهبودی آسان تر است.
بیشتر بدانید؛ آیا قوز قرنیه را می شناسید؟
جراحی پیوند قرنیه چگونه است؟
قبل از عمل پیوند قرنیه پزشک احتمالاً یک معاینه و برخی آزمایشات آزمایشگاهی را انجام می دهد تا از سلامت عمومی شما مطمئن شود. ممکن است مجبور شوید چند هفته قبل از عمل پیوند قرنیه برخی از داروهای خاص مانند آسپرین را متوقف کنید. معمولاً شما باید یک روز قبل از پیوند قرنیه خود از قطره های آنتی بیوتیکی در چشم خود استفاده می کنید تا از بروز عفونت جلوگیری کند. بیشتر اوقات، این جراحی ها به عنوان روش های سرپایی تحت بی حسی موضعی انجام می شود. این بدان معناست که شما بیدار خواهید بود، اما ناراحت کنند نیست، منطقه بی حس است و در همان روز قادر خواهید بود به خانه بروید. پزشک شما تمام جراحی را با میکروسکوپ انجام می دهد. به طور معمول 30 دقیقه تا یک ساعت طول می کشد.
بهبودی بعد از پیوند قرنیه
پس از جراحی پیوند قرنیه، شما احتمالاً حداقل یک روز، شاید 4 روز، چشم خود را خواهید پوشاند تا لایه بالای قرنیه شما بهبود یابد. چشم شما به احتمال زیاد قرمز و حساس به نور خواهد بود. ممکن است برای چند روز احساس درد کنید، اما برخی از افراد هیچ ناراحتی را احساس نمی کنند. پزشک شما برای کاهش التهاب و کاهش احتمال عفونت، قطره چشم تجویز می کند. او ممکن است داروهای دیگری را برای کمک به درد تجویز کند. او می خواهد روز بعد از عمل، چندین بار در طی دو هفته بعد، و سپس چند بار دیگر در طول سال اول، چشم شما را معاینه کند.
برای روش های پیوند مانند DSEK و DMEK که از حباب گاز در داخل چشم استفاده می کنند تا بتواند بافت پیوند شده را قرار دهند، جراح ممکن است از شما بخواهد که در طول روز بعضی اوقات صاف دراز بکشید و شبها روی پشت خود بخوابید. بعد از عمل باید از چشم خود در برابر آسیب محافظت کنید. دستورالعمل های پزشک خود را با دقت انجام دهید. قرنیه شما خون نمی گیرد بنابراین به آرامی بهبود می یابد. در صورت نیاز به بخیه، پزشک شما آنها را چند ماه بعد در مطب از چشم شما خارج می کند.

عوارض احتمالی جراحی پیوند قرنیه
پیوند قرنیه روشی نسبتاً بی خطر محسوب می شود، اما جراحی است، بنابراین خطراتی نیز وجود دارد. در حدود 1 از هر 10 پیوند، سیستم ایمنی بدن به بافت اهدا شده حمله می کند. به این حالت رد گفته می شود. در بیشتر مواقع با قطره های چشم قابل برگشت است. از آنجا که بافت اهدا کننده برای DSEK و به خصوص DMEK استفاده می شود، این روش ها احتمال رد بسیار کمتری وجود دارد. عوارض احتمالی دیگری که ممکن است اتفاق بیفتد شامل موارد زیر است:
- عفونت
- خون ریزی
- فشار بیشتر در چشم (به نام گلوکوم)
- پر شدن مایع چشم (به نام آب مروارید)
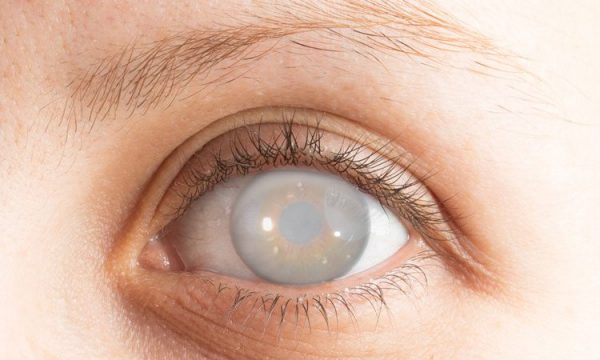
- تورم قرنیه
- شبکیه جدا شده، هنگامی که سطح پشتی چشم شما از حالت طبیعی خود خارج می شود
نتایج جراحی پیوند قرنیه
بیشتر افرادی که پیوند قرنیه دارند حداقل بخشی از بینایی آنها ترمیم می شود، اما نتیجه برای افراد متفاوت است. این امر می تواند چند هفته و حداکثر یک سال طول بکشد تا دید شما به طور کامل بهبود یابد. ممکن است بینایی شما قبل از بهتر شدن کمی بدتر شود. ممکن است نیاز به استفاده از عینک یا تجویز لنزهای تماسی باشد که شامل اصلاح آستیگماتیسم شود زیرا بافت پیوند شده کاملاً گرد نخواهد بود. بعد از سال اول، شما باید سالی یک یا دو بار به چشم پزشک خود مراجعه کنید.
تکنیک جراحی پیوند قرنیه
شرح پیوند قرنیه
غشای آمنیوتیک، یا آمنیون، داخلی ترین لایه چشم است و از یک غشای زیرین ضخیم و یک ماتریس استرومائی آواسکال تشکیل شده است. پیوند غشای آمنیوتیک به عنوان یک پیوند یا به عنوان یک پانسمان در موارد خاص جراحی استفاده شده است. در زمینه چشم پزشکی، از این بافت به عنوان باند بافتی برای عفونت های قرنیه و ذوب استریل استفاده می شود و برای بازسازی سطح چشم از روش های مختلف استفاده می شود.

تاریخ پیوند قرنیه
غشای جنین زنده که شامل هر دو آمنیون و کوریون بود، اولین بار توسط رووس در سال 1940 برای استفاده در بازسازی قرنیه ثبت شد. در طی همان سال، میزان موفقیت بسیار ناچیزی گزارش شد. در همان سال، براون از پاریتونوم خرگوش به عنوان یک ماده موقت برای کاهش سوزش های سطح چشم استفاده کرد که بعداً سورسبی در سال های 1946 و 1947 با غشای آمنیوتیک انسان آن را اصلاح کرد. در 1995 کیم و تسنگ ایده غشای آمنیوتیک را برای استفاده از چشم که آن زمان محبوبیت بیشتری یافته بود، مجدداً معرفی کرد.
مکانیسم عمل پیوند قرنیه
مؤلفه غشای زیرزمین غشای آمنیوتیک در ترکیب با قرنیه مشابه است. به همین دلیل، تئوری فعلی نشان می دهد که تقویت های غشای آمنیوتیک از سلولهای بنیادی لیمبول و سلولهای تقویت کننده قرنیه پشتیبانی می کنند. کلونوژنیسیته حفظ می شود که باعث تمایز سلول های اجباری و غیر غنی می شود در حالی که سلول های التهابی و فعالیت های پروتئاز آنها را از بین می برد. علاوه بر این، تمایز میوفیبروبلاست های طبیعی را کاهش می دهد تا تشکیل اسکار و عروق را کاهش دهد. این عمل به بهبودی برای ترمیم قرنیه، نقص اپیتلیال و زخم استروما کمک می کند.
گزینه های درمانی پیوند قرنیه با غشای آمنیوتیک
AM را می توان با موفقیت به عنوان پیوند قرنیه یا بانداژ استفاده کرد. غشای آمنیوتیک به مدت دو دهه در معالجه چشم پزشکی برای تعدادی از شرایط، مانند پیتفیگوئید سیکاتیریک و سندرم استیونز-جانسون در چشم پزشکی استفاده شده است. pterygium؛ نقص اپیتلیال مداوم با زخم. بازسازی سطح قرنیه؛ و بازسازی سطح چشم در بیماران مبتلا به سوختگی شیمیایی و حرارتی – سایپرز، غشاء شامل سه لایه است: اپیتلیوم. پوسته ی مقر اصلی؛ و استروما. AM دارای خواص ضد التهابی و ضد میکروبی و ایمنی زایی کم است که می تواند برای چشم مفید باشد. احتمال انجماد و حفظ بخشهای غشایی باعث افزایش استفاده بالینی آن شده است.
Scheffer Tseng ، دکترای PhD،مدیر پزشکی مرکز Ocular Surface Surface در میامی می گوید: “استفاده از آن در حال افزایش است و می تواند به دو دسته تقسیم شود.” وی می گوید: می توان از آن به عنوان پیوند جراحی استفاده کرد، جایی که بافت در میزبان قرار می گیرد و می تواند به عنوان یک باند بیولوژیکی مورد استفاده قرار گیرد. هنگامی که به عنوان بانداژ استفاده می شود، بافت داخل میزبان قرار نمی گیرد. در عوض، آن را فقط به عنوان یک پانسمان موقت قرار می دهند. ”
هنگامی که به عنوان پیوند قرنیه مورد استفاده قرار می گیرد، غشای آمنیوتیک داربست مجدداً اپیتلیالیزه را فراهم می کند. دارن گریگوری، دکتر، دانشیار چشم پزشکی در دانشکده پزشکی دانشگاه کلرادو می گوید: “به عبارت دیگر، این پایه است که می تواند پوست را در مواردی که بافت به هر دلیلی از بین رفته باشد رشد دهد.” وی همچنین می افزاید: این ماده همچنین اثر ضد التهابی و ضد زخم ایجاد می کند که باعث می شود مقدار بافت زخم به حداقل برسد. امید این است که رشد بافت جدید ایجاد شود نه فقط پر کردن مناطق آسیب دیده با بافت زخم، زیرا بافت اسکار می تواند مانع از حرکت مناسب پلک و حرکت اشک در چشم شود. ”

اثر ضد التهابی به ویژه در موارد سوختگی شیمیایی یا در بیماران مبتلا به سندرم استیونز-جانسون از اهمیت ویژه ای برخوردار است. دکتر گرگوری می گوید: “در این موارد، اغلب التهاب شدید وجود دارد که دو تا سه هفته طول می کشد.” وی گفت: “بعد از فروکش شدن، می بینیم که سطح زیادی از پوست بر روی سطح چشم از بین رفته است و آن مناطق با بافت زخم پر می شوند. وقتی این جای زخم ایجاد شد، خلاص شدن از شر آن تقریباً غیرممکن است و یک چالش واقعی برای بیماران و پزشکان است. ”
هنگامی که AM به عنوان پیوند استفاده می شود، به طور معمول در جای خود چسبیده یا بخیه می شود و انتظار می رود اپیتلیوم روی آن رشد کند. هنگامی که از آن به عنوان بانداژ استفاده می شود،انتظار می رود اپیتلیوم در زیر آن به جای بالای سطح رشد کند. با پیشرفت بهبودی، غشایی مانند یک زخم از بین می رود. هنگامی که به عنوان بانداژ استفاده می شود، در طی هفت تا 14 روز از بین می رود.
دکتر گریگوری می گوید: “هنگامی که غشاء آمنیوتیک در اواخر دهه 90 برای اولین بار در چشم پزشکی استفاده شد و از نظر تجاری در دسترس قرار گرفت، مردم آن را برای همه چیز امتحان می کردند.” وی گفت: “من از آن با کمی نظم استفاده می کنم زیرا به سندرم استیونز-جانسون کمک می کند. بیشتر و بیشتر در مواردی که نقص اپیتلیال غیر شفابخش در قرنیه وجود دارد،مورد استفاده قرار می گیرد، که می تواند به دلایل مختلف اتفاق بیفتد، اما معمولاً یا با نارسایی سلول های بنیادی قرنیه یا زخم نوروتروفیک که قرنیه از بین رفته است همراه است. که به دلیل یک عمل جراحی مغز و اعصاب، آسیب به اعصاب از ویروس ها یا توموری که عصب سه قلو را تخریب کرده است ایجاد می شود و باعث تخریب قرنیه می شود. ”
نشان داده شده است که در درمان انواع شرایط موفق است. به عنوان مثال، در یک مطالعه انجام شده در ایتالیا با 12 سال پیگیری، 5349 عمل جراحی با موفقیت با استفاده از تکه های غشای آمنیوتیک انجام شد. شرایط درمان شده زخم های قرنیه از جمله کراتیت عصبی بود. کراتیت / اندوفتالمیتیس ؛ pterygium ؛ بعد از كراتوپلاستی، گلوكوم یا آب مروارید ؛ ترومای شیمیایی ؛ کراتوپاتی گاو ؛ نئوپلاسم سطح چشم؛ بازسازی قرنیه و فورنیکس؛ دژنراسیون قرنیه ؛ فرسایش مکرر اپیتلیال ؛ نقص سلول بنیادی لیمبی اولیه و ثانویه ؛ پمفیگوئید غشای مخاطی ؛ دیستروفی ؛ ترومای مکانیکی ؛ سندرم مزمن استیون-جانسون یا سندرم لیل ؛ بازسازی حفره آنوفتالمی ؛ ترومای جسمی ؛ بازسازی پلک ؛ سندرم پارگی اختلال عملکردی ؛ و غیره.
موفقیت یا عدم موفقیت درمان با یک سال پیگیری بعد از عمل انجام شد. موفقیت بر اساس دامنه عمل جراحی و وجود یک یا چند معیار زیر مشخص شد: رفع التهاب؛ تسکین علائم؛ ترمیم اپیتلیوم قرنیه منظم و پایدار و ترمیم تمامیت ساختار چشم. موفقیت جزئی بعنوان دستیابی به تنها دو مورد از معیارهای فوق تعریف شده است. عدم موفقیت به عنوان فقدان همه معیارهای فوق تعریف شده است. شرایط با 100 درصد موفقیت شامل: زخم های قرنیه از جمله کراتیت نوروتروفیک است، بعد از كراتوپلاستی، گلوكوم یا آب مروارید، کراتوپاتی گاو دژنراسیون قرنیه؛ دیستروفی ترومای مکانیکی؛ بازسازی حفره آنوفتالمی؛ بازسازی پلک؛ و سندرم اشک ریختگی.

درمان AM در شرايط زير انجام نشد:
- پمفيگوييد غشاي مخاطي (79 درصد)
- سندرم مزمن استیونز-جانسون یا لیل (62 درصد)؛ و غیره (54 درصد)
- بازسازی قرنیه و فورنیکس (47 درصد)
- نئوپلازی سطح چشم (33 درصد)
- کمبود سلولهای بنیادی لیمبی اولیه و ثانویه (32 درصد)
- تروما جسمی (30 درصد)
- ترومای شیمیایی (24 درصد)
- pterygium ( هشت درصد)
- فرسایش های مکرر اپیتلیال (5 درصد)
این مطالعه نشان داد که اثرات درمانی پس از درمان متغیر بوده و به نوع وضعیت آسیب شناختی تحت درمان مرتبط است. با توجه به نتایج مطالعه، “بهترین نتایج در هنگام استفاده از غشاء برای کنترل التهاب و درد بدست آمد. به طور کلی، میزان موفقیت بالاتر هنگام پیوند غشاء برای نشانه درمانی کلیدی آن، یعنی نقص اپیتلیال مداوم با زخم استروما در بیماران مبتلا به نقص عملکردی سلولهای بنیادی لیمبول انجام شد. در چنین مواردی، این روش باعث افزایش مجدد اپی تلیالیزاسیون در اکثر بیماران و ترمیم یک اپیتلیوم قرنیه پایدار در زخم های ناشی از شرایط مختلف پاتولوژیک می شود. ”
غشای آمنیوتیک با موفقیت در برخی از بیماران در بافت قرنیه گنجانیده شد، و قطعات غشایی برای چند روز پس از عمل قابل مشاهده بود. در این موارد، همانطور که در بالا ذکر شد، این غشاء ویژگیهای داربست خود را نشان داد و یک غشای پایه سالم و دست نخورده فراهم کرد که سلولهای بیمار قادر به تکثیر آن بودند. توماس جان، دکتر، در شیکاگو، می گوید AM اکنون استاندارد مراقبت از درمان سندرم حاد استیونز-جانسون است. علاوه بر این، وی دریافت که غشای آمنیوتیک در درمان نکرولیز حاد سمی، سطح طبیعی چشم و پلک را حفظ می کند و ممکن است از کوری جلوگیری کند.
دکتر جان به همراه همكاران خود، دو مورد اول نكرولز سمی اپیدرمال را كه با پیوند غشای آمنیوتیك تحت درمان قرار گرفتند، منتشر كردند و روشهای جراحی را درگیر كردند. پس از درمان با تریمتوپریم و سولفامتوکسازول برای ویتیت مزمن در این بیمار، هر دو چشم و پلک تحت تأثیر قرار گرفتند. وی تحت لیزر دو طرفه سمبولفارون و همه چسبندگی ها قرار گرفت. وی سپس تحت پیوند دو طرفه آمنیوتیک به کل سطح چشم، به جز قرنیه، قرار گرفت. به دلیل از بین رفتن پوست پلک بیمار، پیوند غشای آمنیوتیک روی هر چهار پلک انجام شد و پیوند نوار غشاء آمنیوتیک در حاشیه پلک ها لازم بود. سیزده سال پس از عمل دو طرفه چشم، هیچ سمبلیفرون، اشک در سطح چشم و 20/20 بینایی اصلاح نشده دو طرفه داشت.
بیمار دوم یک دختر 8 ساله با نکرولیز اپیدرمی سمی شدید همراه با پنومونی مایکوپلاسما بود. وي كراتوكونژونكتيويت دو طرفه، پراكنده، انتشار نقايص اپيتليال قرنيه و سمبولارون دو طرفه داشت. پیوند دو طرفه آمنیوتیک با استفاده از یک حلقه سمفلیفون در چشم چپ انجام شد. در این حالت، پیوند غشای آمنیوتیک هر دو سطح چشمی را محافظت می کند و مانع از انقباض قرنیه بدون چسبندگی پلک ها به سطح چشم می شود. دید مرکزی حفظ شد، و حداقل عروق قرنیه محیطی و زخم قرنیه خفیف تا 34 ماه بعد وجود داشت.
دکتر جان می گوید: “در این موارد، اگر در 10 تا 14 روز اول از غشای آمنیوتیک استفاده نکنید، چشم ممکن است با گذشت زمان از بین برود.” “این همچنین برای درمان سوراخ شدن قرنیه و سایر روشهای ترمیم قرنیه به خوبی کار می کند، و در بیشتر موارد تحت بی حسی موضعی به راحتی قابل انجام است.” با این حال، باید توجه داشت که اگرچه می توان از آن برای درمان شرایط ذکر شده در بالا استفاده کرد، اما برای همه موارد ایده آل نیست. به گفته دکتر گرگوری، اگرچه معمولاً از AM برای جراحی پاتریژیم استفاده می شود، اما در موارد اصلی برداشتن پاتریوم از آن استفاده نمی کند. فواید غشای آمنیوتیک در این بیماران این است که یک روش کوتاه تر است و از نظر فنی جراحی کمتری می خواهد. مشکل این است که وقتی AM استفاده می شود نرخ عود بیشتر است.
یک مطالعه که اخیراً منتشر شده است، عوامل خطر را برای تکثیر مجدد بافت pterygial بعد از برداشتن عمل جراحی و پیوند قرنیه مشخص شده است. این مطالعه شامل 130 چشم بود و در 20 چشم عود مشاهده شد. این مطالعه نشان داد که سن کمتر از 40 سال و پیوند AM به جای اتوگرافت قرنیه از نظر آماری فاکتورهای خطرساز عود بودند. علاوه بر این، این مطالعه نشان داد که کاربرد میتومایسین C حین عمل باعث کاهش عود می شود.
Cryopresered در مقابل کم آبی
چندین روش پردازش برای حفظ غشاها برای مصارف داخلی استفاده می شود. در حالی که نشان داده شده است که غشای آمنیوتیک تازه در کاربردهای بالینی مؤثر است، استفاده از آن خطر قابل توجهی از انتقال بیماری را نشان می دهد. به همین دلیل، روشهای پردازش که ضمن تضمین ایمنی، تأثیر بیولوژیکی آن را حفظ می کنند، مهم هستند. یکی از روشهای آن انجماد سرمازدگی است که شامل انجماد سریع بافت می شود. این “برای حفظ تمامیت ساختاری ماتریس خارج سلولی و عملکردهای بیوشیمیایی درون زا از غشای آمنیوتیک بومی و بافت های بند ناف ایجاد شده است.” در مقایسه، دهیدراته کردن فرایند بسیار سخت تری است و نشان داده شده است که باعث دناتوراسیون پروتئین، از بین رفتن عملکرد و آسیب جبران ناپذیر به زیرساخت ها و خواص مواد بافت می شود.
دکتر Tseng و همکارانش اخیراً ارزیابی کردند که چگونه این دو روش پردازش مختلف بر روی یکپارچگی ساختاری و ترکیب بیولوژیکی مولکولهای سیگنالینگ کلیدی در غشای آمنیوتیک و بافت های بند ناف تأثیر می گذارد . در این مطالعه، آنها به طور مستقیم غشای آمنیوتیک و بافتهای بند ناف را با کمبود آب مقایسه کردند. غشای آمنیوتیک / بافت کوریون با استفاده از روشهای بیوشیمیایی و عملکردی از جمله رنگ آمیزی بافت شناسی و هیستوشیمیایی، اسید بیچین کوننیک، الکتروفورز ژل آگارز، وسترن بلات، ELISA و تکثیر و سنجش مرگ سلول انجام دادند. محققان دریافتند که انجماد حفظ معماری بومی ماتریکس خارج سلولی غشای آمنیوتیک / بند ناف و حفظ کمیت و فعالیت سیگنالهای بیولوژیکی کلیدی موجود در غشای آمنیوتیک / بند ناف، از جمله اسید هیالورونیک با وزن مولکولی بالا، مجموعه سنگین-HA و pentraxin 3 را تشکیل می دهد. بافت های کم آب از نظر ساختاری به خطر افتادند و تقریباً فاقد این اجزای مهم هستند.
بافت منجمد شده به یخچال نیاز دارد و ماندگاری محدودی دارد. دکتر گرگوری می گوید: “اگر در یخچال فریزر منفی 70 درجه سانتیگراد باشد، می تواند حداکثر دو سال نگه داشته شود، اما برای بعضی از آنها فریزرهای تخصصی مورد نیاز است.” “سپس، فرم یخ زده یا کم آب وجود دارد، که به هیچگونه تخصصی احتیاج ندارد. فقط می توان آن را در قفسه نگه داشت و در صورت نیاز از آن استفاده کرد. شما فقط آنرا دوباره آب می دهید نگرانی از این فرم این است که آیا واقعاً تمام اسید هیالورونیک را با پروتئین زنجیره جانبی سنگین حفظ می کند که خاصیت ضد التهابی را فراهم کند. ممکن است که فرم کم آب بدن به اندازه اثر ضد التهابی حفظ نکند. ”
دکتر جان آینده پیوند غشای آمنیوتیک را روشن می داند. وی می گوید: “از نظر نشانه ها، غشای آمنیوتیک منطقه عظیمی را شامل می شود که شامل قرنیه و پلک ها است.” وی گفت: “بیماران، به ویژه بیمارانی که لنز داخل چشم را استفاده می کنند، انتظارات بالایی دارند، از جمله کیفیت بالای بینایی، انحراف کمتر قرنیه و بهبود سریع تر بینایی. نتیجه بصری مطلوب به سطح چشم بستگی دارد. سلامت سطح چشمی در این اواخر در چشم پزشکی واقع شده است و غشای آمنیوتیک، به ویژه یک دستگاه داخلی Prokera، یکی از راه های تقویت و بهبود سطح چشمی به همراه جایگزین های مناسب اشک قبل از انجام عمل جراحی آب مروارید با پریمیوم است. IOL یا جراحی انکسار، به خصوص در بیمارانی که دچار خشکی شدید چشم و یا شرایط چشمی سطح چشم هستند، مورد استفاده قرار می گیرد. ”
Pterygium Excision
پس از برداشتن جراحی با پتریژیم، نقص ملتحمه باقی می ماند. این نقص را می توان به تنهایی برای درمان با قصد ثانویه، به طور مستقیم از طریق بسته شدن اولیه، بخیه شده با پیوند اتو پیوند ملتحمه، و یا با غشای آمنیوتیک پیوند داد. با تزریق استروئید حین عمل در نقص بافت اطراف، پیوند غشای آمنیوتیک دارای عود قابل مقایسه با اتوگرافت ملتحمه می باشد. کاربرد میتومایسین C طبق برخی مطالعات میزان عود را کاهش نمی دهد. گزارشات متناقضی در رابطه با میزان عود پتریژیم بعد از استفاده از غشای آمنیوتیک وجود دارد. غشای آمنیوتیک می تواند در نظر گرفته شود که اندازه نقص عمل برای بسته شدن مستقیم یا اتو پیوند ملتحمه مشکل ساز باشد.
بازسازی سطح ملتحمه
علاوه بر جراحی پتریژیم، پیوند غشاء آمنیوتیک (AMT) برای سایر روشهای بازسازی ملتحمه استفاده شده است. تومورهای ملتحمه برداشته شده و نقص باقی مانده با غشای آمنیوتیک اصلاح شده است. استفاده جراحی از AMT برای تجدید نظر در جای زخم ها و سمفلفرون گزارش شده است. در موارد ابتلا به ملتحمه، که در درمان پزشکی ناکام هستند، از AMT برای بازسازی سطح چشم استفاده می شود. ذوب اسکلر به همراه اسکلرا کاداوریک و پوشاندن AMT با موفقیت زیادی روبرو نشده است. یک گزارش نشان می دهد که یک ترشح ترابکولکتومی می تواند با غشای آمنیوتیک جایگزین شود.
کمبود سلولهای بنیادی لنفاوی
غشای آمنیوتیک در موارد نقص سلولهای بنیادی اندام جزئی و کل قابل استفاده است. در موارد كاهش سلولهای بنیادی لیمبول، به تنهائی آمینا كافی نخواهد بود و باید در رابطه با پیوند سلول های بنیادی آلوژنیك استفاده شود. در مورد از دست رفتن جزئی سلول های بنیادی لیمبول، غشای آمنیوتیک نشان داده است که اپیتلیالیزاسیون را بهبود می بخشد و بینایی را با و بدون پیوند سلولی اندام آلوژنیک بهبود می بخشد. تکنیک های جدیدتر شامل استفاده از سلولهای بنیادی اتولوگ و آلوژنیک است که در آزمایشگاه بر روی غشای آمنیوتیک کشت می شوند و سپس پیوند این بافت ترکیبی را بر روی قرنیه های آسیب دیده شدید که دارای سلول های بنیادی درون زا نیستند، پیوند می دهند.
زخم قرنیه و پیوند قرنیه
غشای آمنیوتیک برای زخم های عفونی و استریل با نازک شدن و سوراخ کردن استفاده شده است. برای زخم هایی که بافت قابل توجهی را از دست می دهند، ممبرین آمنیوتیک ممکن است برای ایجاد ضخامت در نقص در لایه ها استفاده شود. چنین مداخله ای به منظور تأخیر در فعالیت پروتئاز و تأمین بخش عمده ای از نقص به امید بهبود سریعتر و جلوگیری از پیوند قرنیه در نظر گرفته شده است. این می تواند یک اقدام موقتی قبل از پیوند قرنیه یا احتمالاً به عنوان یک درمان دائمی کافی باشد.
روش
بسیاری از گزارشات موجود در پزشکی، استفاده از غشای آمنیوتیک انسانی را که در زمان سزارین از جفت برداشت شده و تا زمانی که استفاده بر روی سطح چشمی حفظ می شوند، نشان می دهد. غشاء آمنیوتیک کریوپروز موجود و معمولاً مورد استفاده قرار می گیرد و خصوصیات بافت شناسی و مورفولوژیکی بافت تازه را حفظ می کند. AMT را می توان با بخیه های قابل جذب یا غیر قابل جذب به سطح چشم چسباند. از چسب بافت بیولوژیکی نیز برای متصل کردن AMT به سطح چشم استفاده شده است.

خطرات
بافت آلوژنیک خطر ضمنی انتقال بیماری عفونی را دارد. به طور کلی، غشای آمنیوتیک از اهدا کنندگان بالقوه تحت سزارین که به دلیل بیماریهای واگیردار غربالگری شده اند، تهیه شده است، از جمله: HIV، هپاتیت و سفلیس. جفت با مخلوطی از محلول نمک متعادل، پنی سیلین، استرپتومایسین، نئومایسین و آمفوتریسین B تمیز می شود. آمنیون توسط قطعه شکاف در شرایط استریل، جدا شده در کوریون جدا می شود و به نوارهای کاغذ نیتروسلولوز متصل می شود و در محلول گلیسرول ذخیره می شود. این بافت یا برای استفاده تازه در آن محلول ذخیره می شود یا در دمای 80- درجه سانتیگراد محافظت می شود. در حال حاضر، هیچ گزارشی در مورد انتقال بیماری های واگیر از AMT منتشر نشده است.
یک گزارش از وجود هیپوپیون استریل پس از پیوند مکرر غشای آمنیوتیک انسان بر روی سطح قرنیه وجود دارد. برخی از بیماریهای قرنیه را می توان با پیوند غشای آمنیوتیک درمان کرد. در موارد نقص مداوم اپیتلیال، ذوب قرنیه و اسکلرال، کراتوپاتی گاو و کمبود سلولهای بنیادی لیمبول مفید است. غشای آمنیوتیک این مزیت بزرگ را دارد که به راحتی قابل دستیابی است. هنگامی که برای اهداف چشم پزشکی استفاده می شود، از جفت به دست آمده از طریق سزارین انتخابی گرفته می شود و در حداکثر شرایط استریل نگهداری می شود.
نقص اپیتلیال مداوم با پیوند قرنیه
از غشای آمنیوتیک در درمان نقص مداوم اپی تلیال ثانویه تا قرنیه های عصبی، اختلالات خود ایمنی یا نقص سلول های بنیادی لیمبول استفاده شده است. در این موارد، غشای آمنیوتیک ممکن است با مهار کلاژنازها عمل کند و در عین حال، یک کلاژن و یک غشای زیرزمین را برای رشد سلولهای اپیتلیال فراهم کند. غشای آمنیوتیک همچنین فاکتورهای رشد را فراهم می کند، که همه اینها جو مساعد برای رشد سلول های اپیتلیال را فراهم می کند. همچنین:
مطالعه اثربخشی غشای آمنیوتیک برای خشکی چشم را نشان می دهد. VIDEO، غشای آمنیوتیک انجماد شده فرآیند احیا را تحریک می کند. غشای آمنیوتیک Cryopreservation التهاب را کنترل می کند، باعث بهبودی می شود. قرنیه و اسکلر ذوب می شود. غشاء آمنیوتیک در صورت ذوب قرنیه یا اسکلر به عنوان پیوند لکه دار یا لایه پوششی استفاده می شود. از آن برای پر کردن نقص و جایگزینی از بین رفتن ماتریس استروما ناشی از ذوب استفاده می شود. این کار با استفاده از غشای آمنیوتیک چند لایه انجام می شود.
غشای آمنیوتیک بارها و بارها با استفاده از چسب فیبرین به خود چسبانده می شود تا لایه های چندگانه را به یکدیگر بچسباند. پس از تهیه این لایه، پایه و لبه های ناقص بریده می شوند و تمام بافت های نکروتیک و همچنین اپیتلیوم شل برداشته می شوند. سپس از این لایه برای پر کردن نقص استفاده می شود و با استفاده از چسب و همچنین بخیه های لنگرگاهی در جای خود قرار می گیرد. سپس از یک لایه غشای آمنیوتیک یا پیوند رویشی برای پوشاندن پیوند اینتلی به گونه ای استفاده می شود که فراتر از اپیتلیوم گسترش یابد. این پوشش اثرات ضد التهابی را فراهم می کند و باعث بهبودی زخم می شود.

میکروسکوپ کانفوکال پرکننده غشای آمنیوتیک پیوند شده، انقباض آن را نشان می دهد، با تشکیل کلاژن جدید و جمعیت آن توسط سلولهای مشتق شده از استروما قرنیه حدود 3 ماه، بازسازی شده و دلالت بر ادغام پیوند داخل پرکننده در ماتریس قرنیه دارد. مجدداً اپیتلیال شدن غشای آمنیوتیک برای ادغام پیوند به استروما ضروری است. در حالي كه در بيماري اسكلرا، ادغام با استروماي اسكلروال معمولاً روند بيماري را متوقف مي كند. در قرنیه، پیوند قرنیه به عنوان زخم در استروما ادامه می یابد. با این وجود، آن هنوز هم قرنیه را با چشم پانسمان شده در معرض پیوند آینده قرار می دهد.
مطالعات خاص نیز از این تکنیک در زخمهای بسیار عمیق و سلول های بنیادی استفاده کرده اند. استفاده از غشای آمنیوتیک به تنهایی در موارد زخم قرنیه با عفونت فعال کافی نیست و باید از این کار اجتناب کرد. همچنین ممکن است در مواردی که نواحی بزرگی از ذوب اسکلر با تشکیل استافیلوما یا در زخمهای بزرگ قرنیه وجود دارد که در آن از بافت هایی با حمایت تکتونیکی بیشتری مانند پیوند تکتونیکی قرنیه یا اسکلرال استفاده می شود، به خودی خود نتواند حمایت تکتونیکی داشته باشد. در مواردی که ذوب اسکلرال و نکروز در حال انجام است، مدیریت پزشکی دیگری که به آسیب شناسی بیماری منجر می شود نیز لازم است.
کراتوپاتی بولوز پیوند قرنیه
کراتوپاتی بولوز ثانویه به عمل جراحی یا دیستروفی فوچس در چشم پتانسیل بینایی ندارد و با پیوند غشای آمنیوتیک قابل درمان است. غشای آمنیوتیک ممکن است بعد از برداشتن اپیتلیوم ناسالم یا همراه با سوراخ استروما قدام یا کراتکتومی فوتوتراپی به عنوان درمانی جدا استفاده شود. غشاء تحت فشار قرار گرفته و بر روی قرنیه با استروما رو به پایین بخیه می شود. در این موارد به عنوان جایگزین مناسبی برای درمان ملتحمه عمل می کند و همچنین نتایج زیبایی بیشتری را نسبت به فلپ ملتحمه به بیمار ارائه می دهد. همچنین، بر خلاف فلپهای ملتحمه، در صورت لزوم شانس بقای یک جراحی پیوند قرنیه در آینده را کاهش نمی دهد.
بیشتر بدانید؛ آیا قوز قرنیه باعث انحراف چشم میشود؟
کمبود سلولهای بنیادی لنفاوی
سلولهای بنیادی لیمبل مسئول دوباره پر کردن سلولهای اپیتلیال قرنیه هستند و ممکن است از طریق فرضیه X ، Y ، Z از Thoft و Friend اتفاق بیفتد.
نقص سلول بنیادی لیمبی جزئی
از غشای آمنیوتیک می توان در نقص سلول های بنیادی لیمبول جزئی به عنوان یک روش درمانی جدا شده استفاده کرد. روی سطح قرنیه و ملتحمه پخش شده و در محل با استفاده از بخیه هایی با یا بدون فیبر لنگر استفاده می شود. این ممکن است به دلیل خاصیت منحصر به فرد آن باشد که در مطالعات آزمایشگاهی افزایش طول عمر سلولهای اجدادی قرنیه و ملتحمه و حفظ سلولهای نگهدارنده مشخص شده است. بنابراین می توان از آن برای گسترش سلولهای بنیادی بقایا و سلولهای تقویت کننده گذرا از قرنیه استفاده کرد.

مراقبت های پزشکی بعد از جراحی پیوند قرنیه
بعد از عمل پیوند قرنیه، آنتی بیوتیک ها، هیالورونات سدیم و قطره های چشمی میردریت به همراه پماد چشم آنتی بیوتیک تجویز شد. پس از برداشتن بانداژ، برای بیماران مبتلا به زخم قرنیه غیر قارچی، 0.5 درصد قطره چشم لووفلوکساسین (Cravit،شرکت دارویی سانتن، اوزاکا، ژاپن)، 0.1 درصد قطره چشم فلورومتولون (Flumetholon، شرکت دارویی سانتن، اوزاکا، ژاپن)، 0.1 درصد سدیم قطره چشم هیالورونات (Hyalein 0.1، شرکت داروسازی سانتن، اوساکا، ژاپن) و قطره چشم 5/0 درصد تروپیکامید (Shuangxingming، شرکت دارویی Zhenshiming ، Fuzhou، چین) 4 بار در روز تجویز می شود. قبل از خواب 0.3٪ پماد چشم افلوکساسین (Dikeluo، شرکت داروسازی Xinqi ، Shenyang، چین) استفاده شده است.
برای بیماران مبتلا به زخم قرنیه قارچی، 1/0 قطره چشم فلورومتولون (Flumetholon،شرکت داروسازی سانتن، اوزاکا، ژاپن) با 5 درصد قطره چشم ناتامینایسین جایگزین شد، برای استفاده 6بار در روز. هر بیمار را روزانه در هفته اول بعد از عمل، و پس از آن هفته ای یک بار به مدت 3 ماه بعد از عمل در زمان های مناسب پیگیری کردیم. در طول پیگیری ها، حدت بینایی و فشار داخل چشم (IOP) اندازه گیری شد و معاینات شکاف لامپ برای ارزیابی میزان بهبود زخم قرنیه، یکپارچگی پیوند، علائم التهاب، عفونت و تغییر در سطح چشم و همچنین برای نظارت بر تغییرات AMR انجام شد.
اگر حدود 1 هفته پس از عمل، روکش پیوند بزرگ موقت AM شل یا حل شد،ما آن را از بین بردیم. یک ماه پس از هر عمل، در هر پیگیری با UBM یا توموگرافی انسجام نوری (OCT) برای ارزیابی وضعیت فیوژن AMR و سازمانهای قرنیه در 33 بیمار اندازه گیری شد. موفقیت جراحی به عنوان قطع اشک چشم، نتیجه منفی آزمایش سییدل، اپیتلیالیزه شدن کامل لایه بیرونی AM و تشکیل ضخامت استروما قابل مشاهده در محل عمل تعریف شد. نارسایی جراحی به عنوان تداوم یا عود اشک چشم، عدم وجود اپیتلیالیزاسیون یا زخم مکرر قرنیه تعریف شده است.